限制性内切酶克隆
概述了限制性内切酶克隆背后的科学,以及如何在衍因智研云中模拟限制性内切克隆。
什么是限制内切酶克隆?
分子克隆包括复制DNA片段的多个拷贝,以便于后续的研究和操作。实现克隆通常需要将感兴趣的DNA片段(也称为“插入片段”)插入到一个环状自我复制的DNA分子中,该分子被称为质粒载体。一旦DNA片段插入到质粒中后,可以将其转化进细菌感受态中,随即在细菌自我复制,每个细菌可以产生数百个相同的“克隆”拷贝。
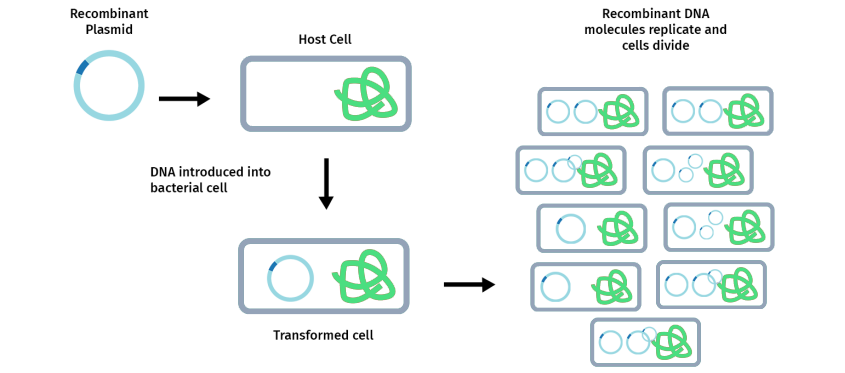
质粒在细菌中的复制
限制性内切酶克隆,也称为"限制性克隆",是一种利用DNA限制性酶在特定位置对载体和插入片段进行切割的技术,通过切割后的末端与DNA连接酶的作用,载体和插入片段可以被连接在一起,形成重组DNA。这种方法可以用于插入特定的DNA序列到目标载体中,从而实现分子克隆。
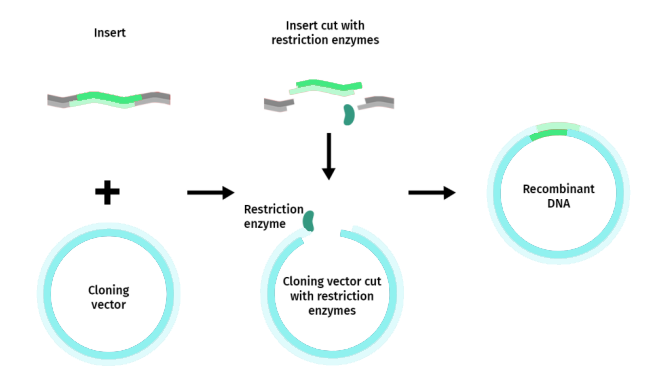
Recombinant DNA(重组DNA)
限制性克隆的历史与应用
在20世纪70年代之前,科学家们无法轻松地分离和研究单个基因。随着限制性内切酶和DNA连接酶的相继发现,再加上相关科学方法的发展,使得科学家们能够利用这些工具从基因组中分离出单个基因。

因发现并应用限制酶而获得1978年诺贝尔生理学或医学奖的三位科学家

瑞典1989年发行的诺贝尔奖纪念邮票。票面为限制酶切割DNA分子示意图,左下方有三位获奖者的名字
该领域的第二个重大突破是发展出能够接收和复制的分离DNA片段的质粒克隆载体,这些工具的开发促成了1972年首个重组DNA分子的问世。
将基因克隆是为了使其编码的蛋白质能够高水平表达并进行纯化,进而应用于医学、实验或商业用途。
1978年,人类胰岛素在细菌中成功克隆和表达。CRISPR酶Cas-9被克隆到多种特定生物的载体中,使得基于CRISPR的基因编辑技术可以在这些生物体内得以应用。为了增强植物对环境中的病原体或有毒化学物质的抗性,人们将克隆的基因引入植物中。限制性酶克隆和子克隆是多年来分子生物学领域的主要技术。事实上,超过70%的分子生物学实验都是从限制性酶切克隆DNA片段开始的。
设计规划限制性克隆实验
选择载体系统
下述质粒展示了限制性克隆载体所需的必要特征:
复制起点(ori):复制起点的存在使得克隆后的重组DNA载体能够在宿主基因组中独立进行复制。
选择标记物:选择标记物使得选择性生长试剂能够确保生长的细菌中含有目标载体。在细菌中,常用的选择标记物是某种抗生素抗性基因,例如氨苄青霉素抗性(Ampr)、卡那霉素抗性(Kanr)。通过将抗生素抗性基因与目标DNA重组,可以使得克隆后的DNA在宿主基因组中独立进行复制,并通过抗生素筛选出带有目的DNA序列载体的细菌。
方便插入位点:在利用限制性酶进行克隆时,通常将目的DNA片段插入多克隆位点(MCS)。MCS是一组具有多个不同限制性酶的切位点集合,可以用来插入目的片段。
克隆选择标记:一个表明载体中含有插入DNA的标记物。
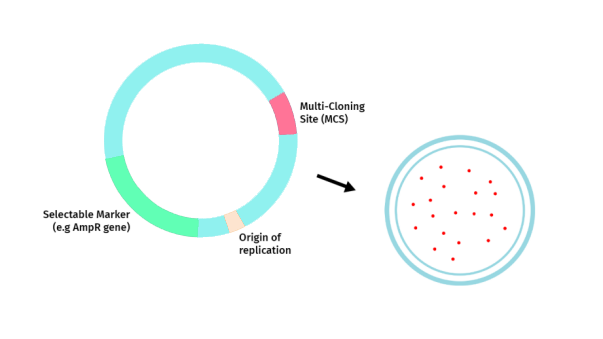
选择载体系统
载体的选择还取决于后续对质粒的操作计划,以及选用的宿主生物体用于表达分子克隆。许多质粒经过预先设计,可以接受目标片段,并添加了各种功能性基因,例如用于纯化的多肽标签、亚细胞定位序列,或用于辅助观察蛋白质表达位置的荧光蛋白标签。
限制酶的类型
ⅡP型限制酶是分子生物学领域中的重要工具,由于它们能够识别和结合特定的DNA序列,并且无论DNA的来源如何,总是在相同的位置进行酶切。因此,ⅡP型限制酶长期以来一直被广泛应用。
这种酶切会产生三种主要类型的“酶切末端”:
5'黏末端:产生一段未配对的5' DNA序列
3'黏末端:产生一段未配对的3' DNA序列
平末端切割:不产生未配对的DNA序列
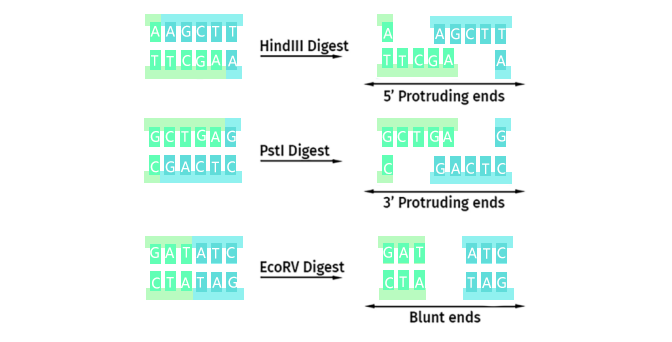
限制酶切位点末端
一旦完成酶切,DNA的两端就会成为DNA连接酶的作用底物。带有黏末端的DNA将会与互补的末端连接,形成稳定的沃森-克里克碱基配对。而所有的平末端则可以相互兼容。
单酶切或双酶切克隆
根据可用的克隆位点和插入片段的方向,克隆策略可以选择单酶切克隆或双酶切克隆。
在单酶切克隆中,可以使用相同的限制酶来切割载体和插入片段。这种方法通常适用于对要克隆的DNA片段的方向要求不高的实验,比如构建基因组DNA文库或cDNA随机裂解文库。单酶切消化的目的是从给定的基因组DNA或cDNA中分离出许多不同的片段。
双酶切或定向克隆使用两种不同的酶。定向克隆可确保插入的片段以指定的方向引入,并减少由于线性载体自身闭合而产生的背景菌落。示例包括将基因或 cDNA 定向克隆到载体中。
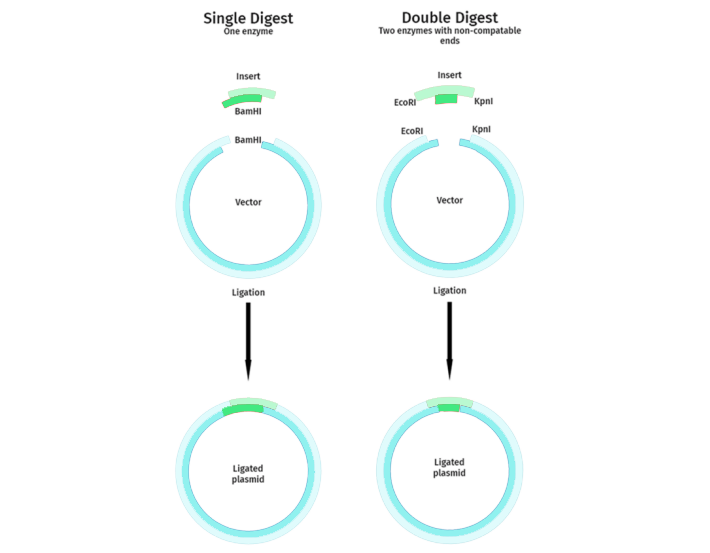
单酶切与双酶切
酶的位置
酶与线性 DNA 分子末端的相对位置也很重要。大多数酶需要识别位点附近有 4 到 6 个碱基对来稳定 DNA,从而实现有效切割。如果两个酶位点距离太近,则一种或两种酶会互相影响,导致无法有效切割。
限制性内切酶克隆法的优缺点
限制性酶克隆有许多优点:
1、该方法具有丰富的资源库,从操作步骤到商业和学术资源,如载体和细菌系统。
2、它已被广泛了解和研究——从高中到大学都在教授这种方法。
3、存在多种具有不同识别位点和潜在末端的限制性酶,这些酶已被广泛使用。
4、有多种分子生物学软件可以帮助您进行设计和实验规划。
限制性酶克隆虽然很流行,但也存在一些缺点:
1、该方法耗时较长,涉及多个步骤,通常需要连续几天才能完成克隆。
2、若设计针对阅读表达框研究的实验时,需要必须特别小心。
3、必须确保您选择的限制性内切酶能够使目的片段以正确的方向插入到载体中。
何时应该使用限制性内切酶克隆?
以下是一些适用限制性内切酶克隆的情况:
· 您希望利用多种载体和表达系统进行实验。
· 您希望证明自己可以成功使用分子生物学中最广泛使用的克隆方法完成实验。
· 您希望能够根据实验设计自由规划和构建克隆载体。
· 随着实验需求的增长,您希望可以方便地重复使用克隆来构建更复杂的结构。
成功进行限制性酶克隆的 7 个技巧:
1、谨慎选择酶的组合,确保其在插入片段和载体中具有唯一识别的酶切位点。
2、如果您正在设计一个表达实验,请确保目的片段与所使用载体的 N 端和 C 端元件在同一框架内。
3、尽可能执行定向克隆。
4、使用凝胶电泳方法纯化你的片段,并在NanoDrop上准确定量,凝胶电泳是去除小片段和未切割载体最有效的方法,近乎100% 的纯化效率。
5、在连接时,采用不同的插入片段与载体摩尔比。大多数连接反应在2:1到3:1范围内效果较好,而对于平末端连接和非常小的插入片段则在更高的摩尔比(10:1到20:1的范围内)下效果更佳。你可以使用在线的摩尔比计算器,轻松计算出需要多少DNA来达到你所期望的摩尔比。
6、确保连接缓冲液完全解冻并充分混匀。
7、对分子克隆的关键区域进行测序验证。
在衍因智研云中模拟限制性克隆
通过使用软件,您可以精确地设计和模拟限制性克隆过程。这种软件能够帮助您在实验前进行预测,从而在正式实验中避免错误,确保成功构建出所需的载体。这一过程尤其适用于复杂的构建工程。
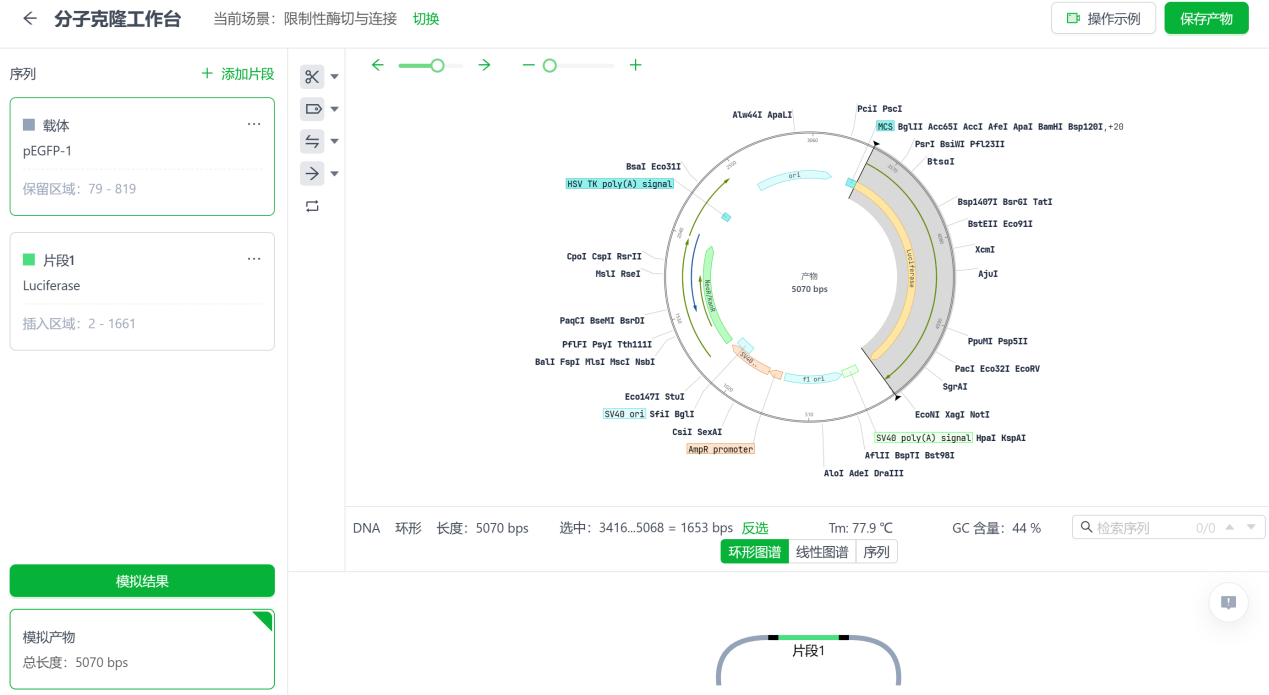
衍因智研云质粒库中有数千个质粒,可轻松直接添加到您的克隆实验中。或者,可以将质粒序列复制并粘贴到软件中。
一旦完成导入,软件就会提供多种注释选项,可用于可视化和验证所有质粒元件,包括编码蛋白质的元件。